SOLUBILIDAD DEL HIERRO
BLOG PREMIUM DEL LABORATORIO DE FORJA
SOLUBILIDAD DEL HIERRO
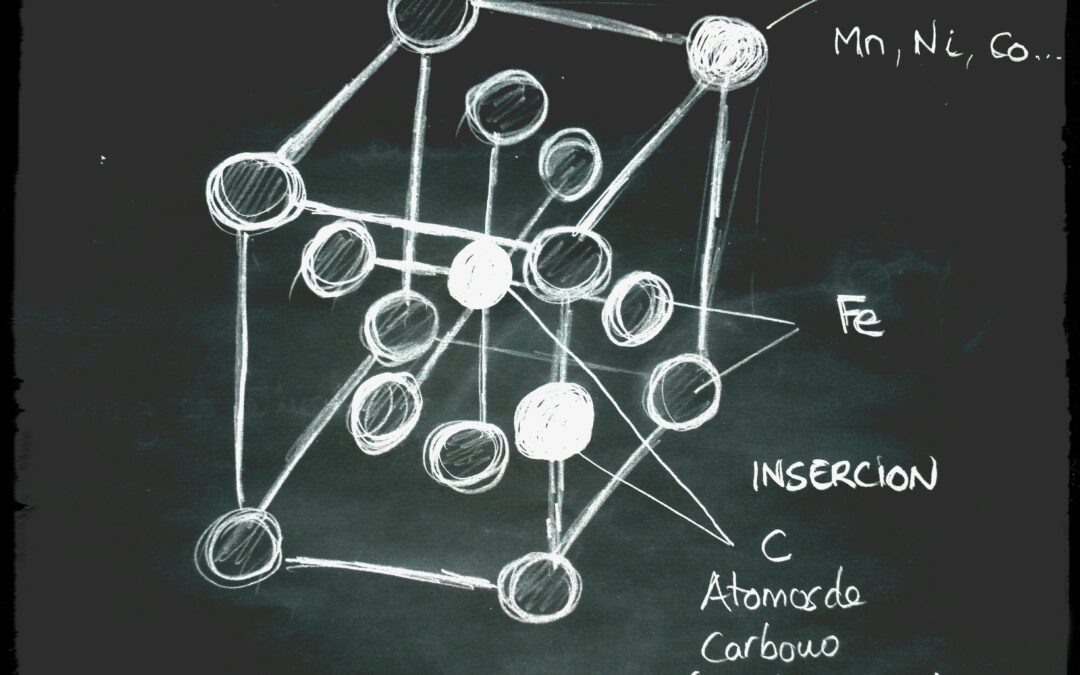
Si los átomos de los elementos de aleación que tiene el acero para modificar sus propiedades mecánicas son de pequeño radio atómico, estos elementos se insertan entre los espacios existentes entre los átomos de hierro. Si los átomos de estos elementos son mayores, pueden llegar a sustituir a los átomos de hierro.
ON EL MICROSCOPIO:
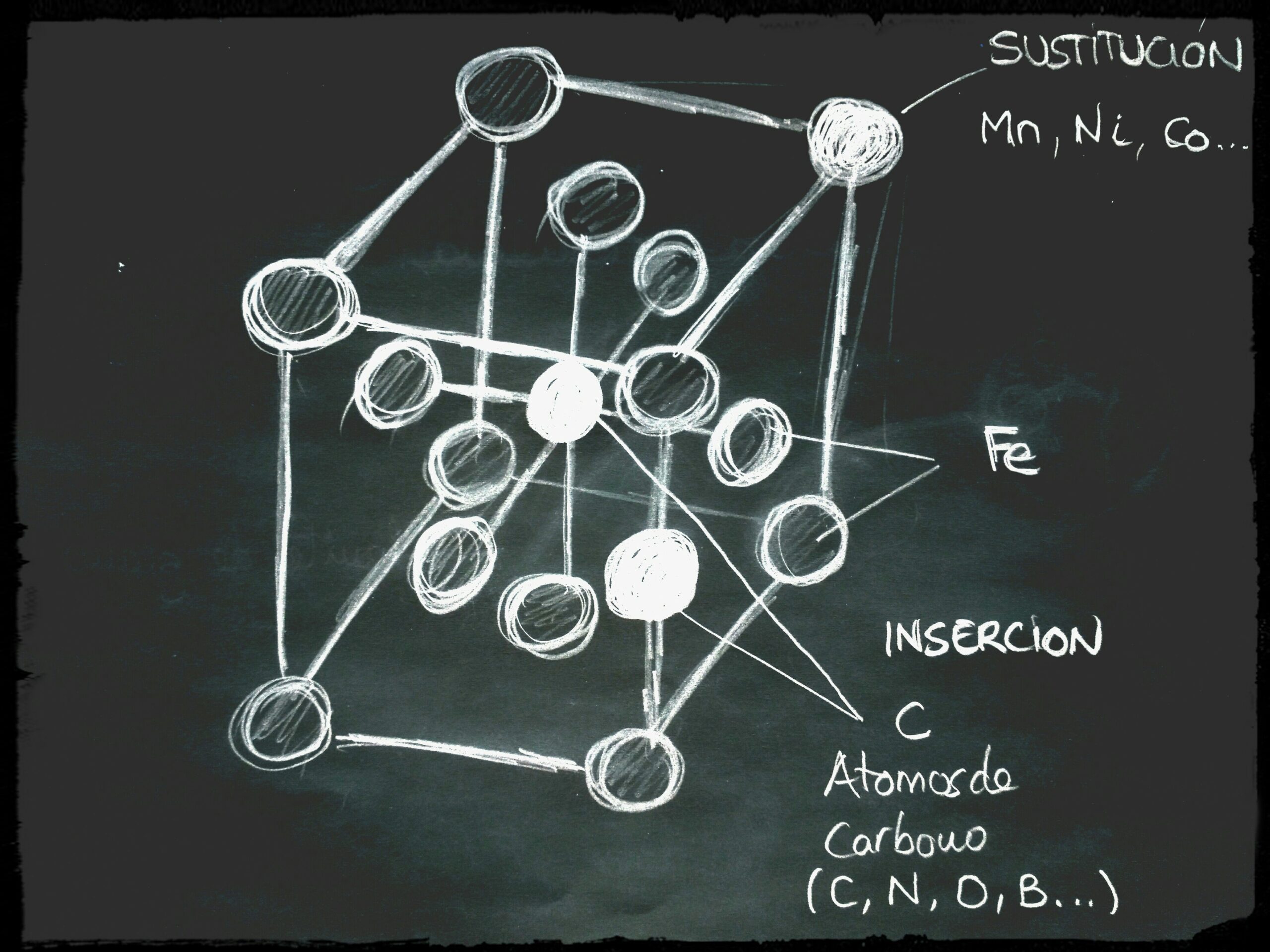
Soluciones sólidas de sustitución:
Hay elementos que sustituyen aleatoriamente a los átomos de Hierro (Fe) en su red cristalina como es el caso del Manganeso (Mn), del Niquel (Ni), del Cobalto (Co)…
Soluciones sólidas de inserción:
Si los átomos son de pequeño radio atómico <0.1 nm (nanómetros), como con el Carbono, además del Hidrogeno (H), el Oxigeno (O), el Nitrógeno (N), del Boro (B)… no sustituyen a los átomos de Fe, sino que se insertan en los espacios que hay entre los átomos de hierro.
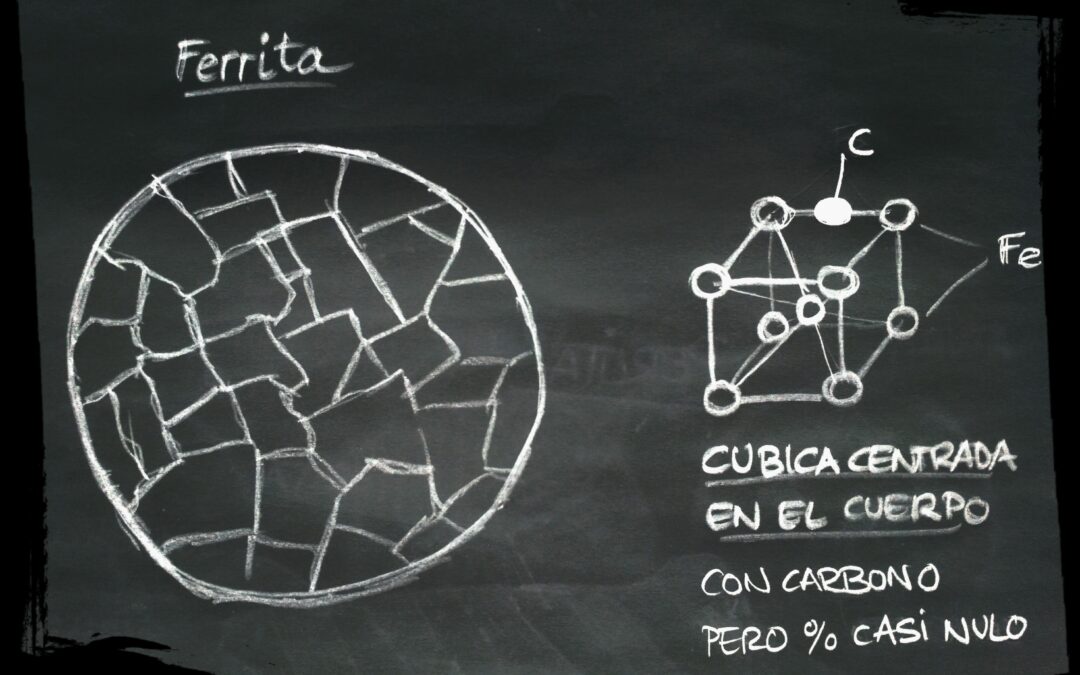
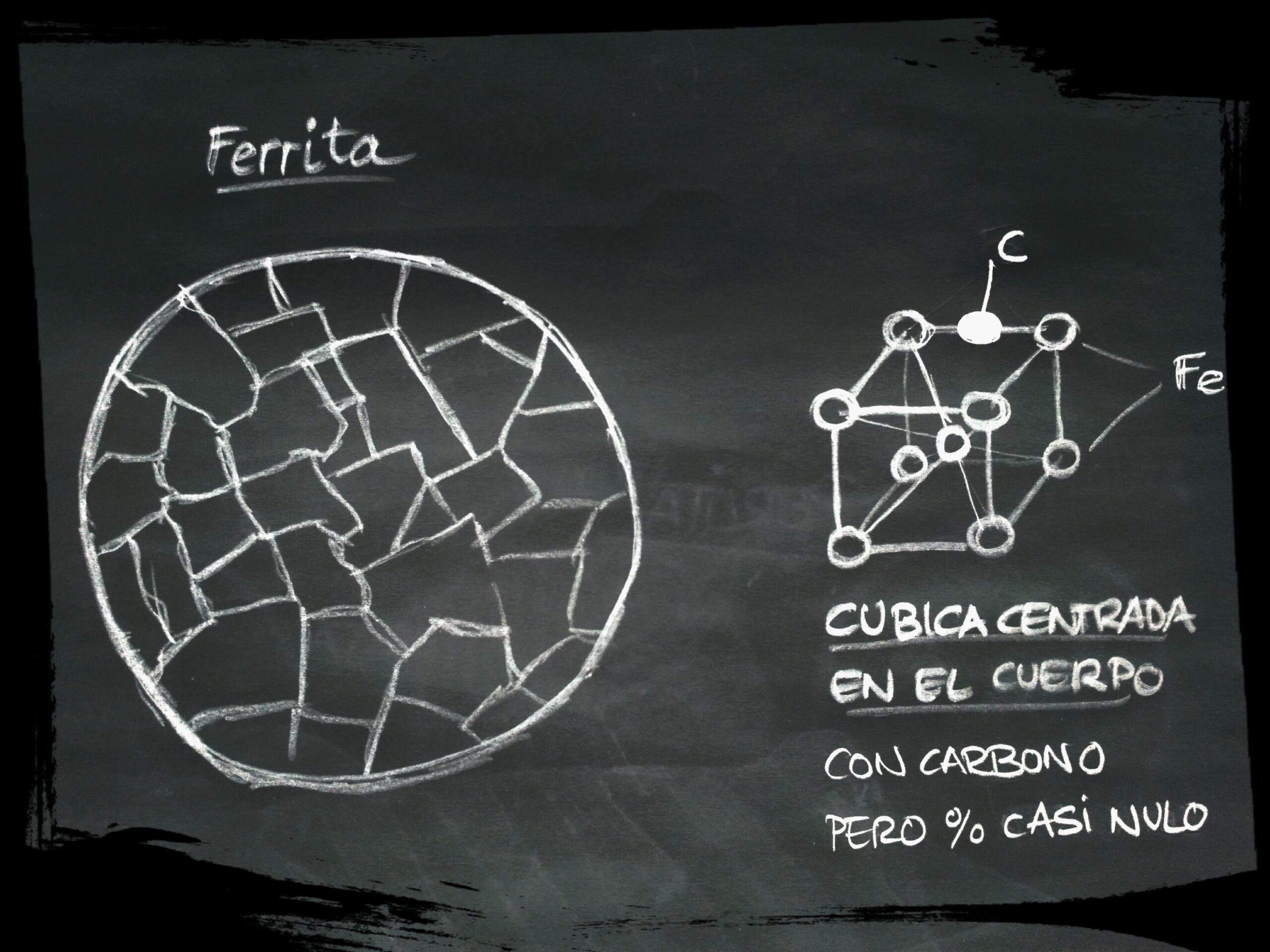
Los átomos de carbono se introducen en los huecos existentes entre los átomos de hierro. Alojándose el carbono en el centro de las aristas y en el interior del cubo. A temperatura ambiente la solubilidad del Carbono en el hierro es muy, muy pequeña.
La tamaño del hueco entre los átomos de hierro depende de su estado cristalino, siendo la solubilidad del hierro gamma (912ºC – 1388ºC) mayor que la del hierro alfa (hasta los 912ºC). Esta carácteristica la aprovecharemos para modificar las propiedades mecánicas de los aceros.
¿TODOS LOS ELEMENTOS DE ALEACIÓN ESTAN DISUELTOS EN LA ESTRUCTURA CRISTALINA DEL HIERRO?
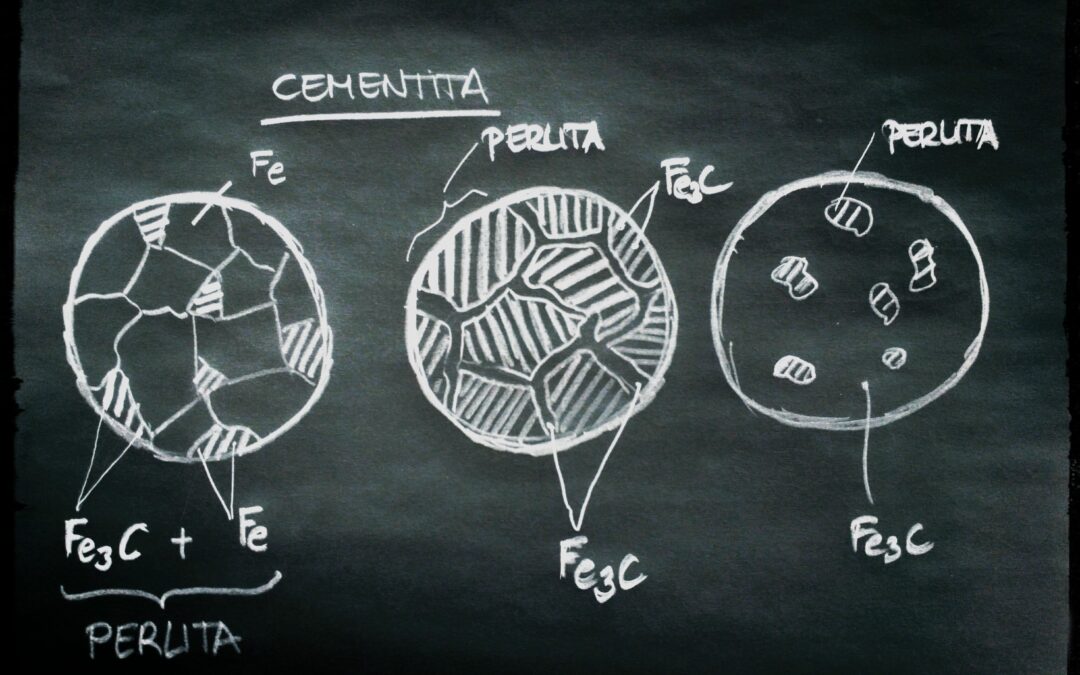
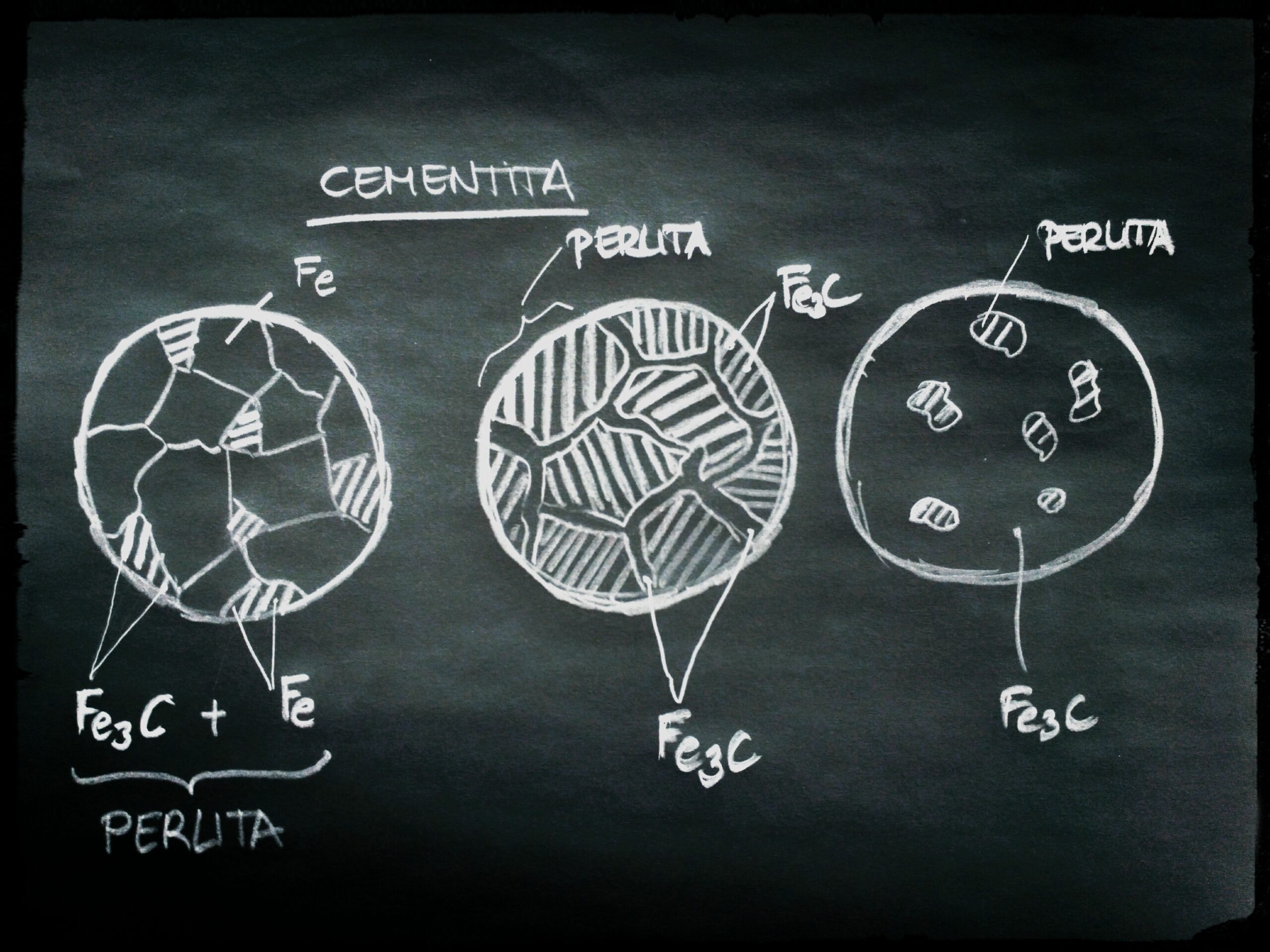
En el acero, podemos tener la presencia de elementos de aleación disueltos en la estructura cristalina del hierro, pero también en forma de carburos (aportan dureza y fragilidad). Esto depende de la composición química del acero y del proceso de tratamiento térmico al que ha sido sometido y de la temperatura.
Algunos elementos de aleación tienden a formar carburos de manera más predominante en ciertas condiciones de tratamiento térmico o en composiciones específicas del acero.
A temperatura ambiente, la presencia de carburos puede variar dependiendo de la velocidad de enfriamiento durante el forjado o tratamiento térmico. Si el enfriamiento es lo suficientemente rápido, es posible que no se forme una cantidad significativa de carburos, lo que podría permitir que más elementos de aleación queden disueltos en la estructura cristalina del hierro.